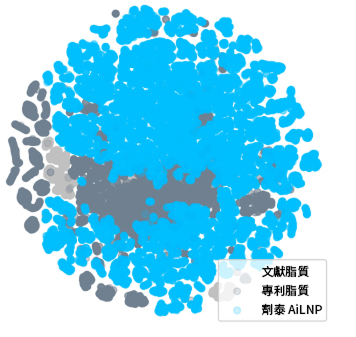
試想一種藥物能像智慧手機安裝APP般自由升級——這正是"可程式設計藥物"創造的醫療革命。不同于傳統藥物僅靠化學鍵被動生效,這種創新療法通過合成生物學與AI雙引擎驅動,將DNA/RNA片段編譯成"基因軟體",借助納米級智慧載體精准植入細胞,實現對生命程式的改寫與優化。
在微觀世界中,CRISPR-Cas9系統猶如精准的基因剪刀,搭載到脂質納米顆粒(LNP)組成的"納米火箭",就可將定制化DNA範本精准靶向遞送到病變細胞核。當AI預測模型識別到特定疾病信號,預先程式設計的mRNA鏈便開始"轉錄-翻譯"接力:核糖體工廠高效合成治療性蛋白質,如同批量生產微型機器人,既能清除錯誤折疊的致病蛋白,又能啟動休眠的抑癌基因。
隨著科研的不斷突破,未來“可程式設計”藥物也許可以給細胞裝上可程式設計“晶片”,“一鍵重啟”疾病細胞回到健康細胞。科學家正在構建涵蓋基因編輯、表觀遺傳修飾、蛋白質合成的全維度調控網路,未來或可像調試電腦代碼般,為阿爾茨海默症患者重建記憶回路,為漸凍症患者啟動運動神經元,真正實現疾病的個性化、數位化診療。
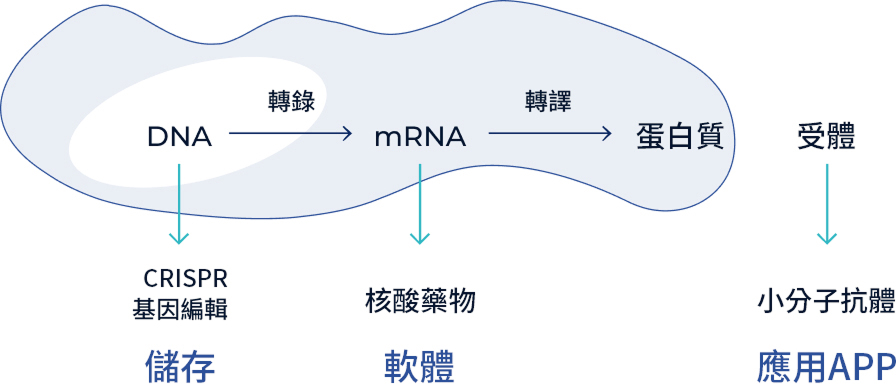
mRNA, 即信使核糖核酸(Messenger RNA),是一種攜帶遺傳信息的分子,作為DNA和蛋白質之間的橋樑,指導蛋白質生產。理論上,科學家可以利用mRNA合成任何想要的蛋白質,來達到治癒疾病的效果。
在生命劇場中,mRNA扮演著"動態樂譜"的角色——它將DNA中靜態的遺傳密碼翻譯成蛋白質的動態交響曲。而可程式設計藥物通過AI演算法重構這段"樂譜",讓mRNA化身精准的"分子建築師",在細胞內按需搭建功能元件。
科學家利用化學修飾技術為mRNA穿上"隱形斗篷",使其避開免疫系統的追查;再通過納米脂質體構建"納米火箭",搭載編碼特定功能蛋白的mRNA序列直抵病灶。當納米載體感知腫瘤微環境的低氧信號時,會自動釋放mRNA,指揮細胞工廠生產抗癌蛋白。
這種技術已在臨床試驗中展現驚人潛力:編碼Cas9蛋白的mRNA與嚮導RNA組成"基因剪刀套裝",可精准切除致病基因並替換為健康版本;針對罕見病的mRNA療法甚至能重啟胎兒期的血紅蛋白合成通路,替代有缺陷的成人血紅蛋白。未來,結合AI預測模型,mRNA或將具備即時感知疾病進程的能力,像智慧溫控系統般動態調節治療劑量,實現真正的按需醫療。
“可程式設計細胞”的未來,讓科學家們遙望一個沒有疾病,沒有衰老的世界,而通往這個世界的必經之路離不開納米遞送技術。
mRNA是個嬌嫩的"棉花衛星",既怕核酸酶撕碎,又因負電荷無法穿透細胞膜,需要得到LNP“納米火箭”超能力的精准護航。LNP可以為其量身打造三層防護:外層PEG脂質偽裝成無害脂蛋白騙過免疫系統,中層可電離脂質化身"變形金剛",在胃酸中蜷縮成緻密球體保護貨物,進入細胞後遇鹼性環境瞬間展開,像"分子爪"般釋放mRNA。
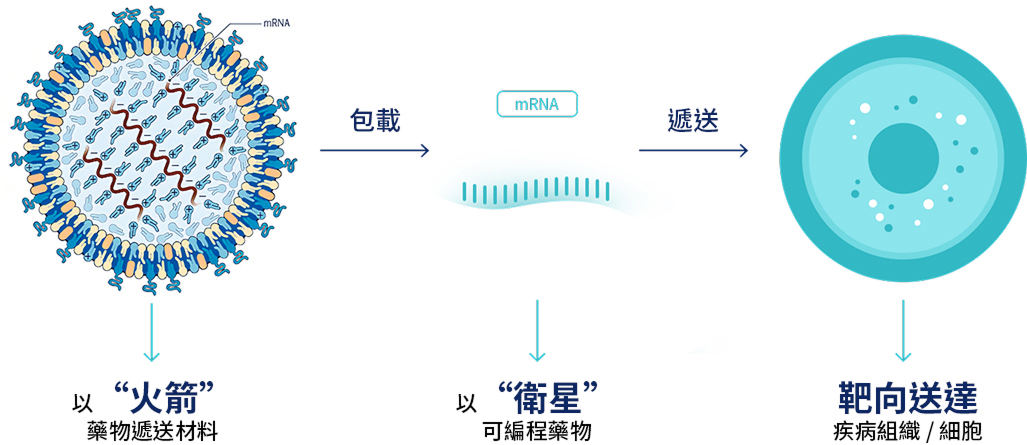
未來的藥物將以基因編碼指令為核心,通過核酸藥物遞送系統實現疾病細胞的精准重程式設計。這類"可程式設計藥物"以“火箭+衛星”的模式,要依靠特定的LNP納米載體“火箭”,搭載mRNA或CRISPR-Cas9系統等特定遺傳信息的核酸分子“包裹”,才能實現靶向遞送與可控釋放。
LNP的技術顯著提高了mRNA的有效性和安全性,輝瑞/BioNTech與Moderna的兩款mRNA疫苗均採用LNP遞送,為控制全球大流行立下了汗馬功勞。2022年,開創LNP藥物遞送工作的皮特·庫裡斯(Pieter Cullis)、卡塔琳·卡裡科(Katalin Karikó)、德魯·魏斯曼(Drew Weissman)獲得素有“小諾貝爾獎”的蓋爾德納獎。
LNP(脂質納米顆粒)通常至少有四種不同的脂質成分。每一種成分都具有獨特的化學結構和不同的物理化學性質,並可以彼此獨立地被優化。當所有這些可能的變數疊加時,會出現一個非常大而複雜的空間,找到最佳組合,幾乎就像大海撈針。
這些關鍵的最優空間實際上可能是不連續和分散的,這意味著如果使用傳統的DOE方法,篩選相對較小的空間有可能找到局部最優,但同時很可能錯失篩選能力之外的最佳空間。圖中可以看到文獻或專利中所有已知的脂質,許多點傾向於聚集在一起,因為傳統方法往往互相學習,互相借用前人或對方的結構。但真正引人注目的是圖中間的大量空白。
從成立的第一天開始,劑泰科技就想做一些非常不同的事情。我們希望能夠應用人工智慧機器學習工具,然後與高通量篩選、實驗平臺相結合,建立傳統雷達之外的藍色大海,填滿整個空間。創立5年以來,劑泰首創了AI納米基座大模型,率先實現人工智慧端到端脂質設計。相比于傳統模式,AI説明我們將納米遞送材料設計空間擴展了千倍以上。